
幹細胞とは?
幹細胞について
今回は、幹細胞の基礎から最新の研究動向まで詳しく解説します。
ES細胞、iPS細胞、再生医療への応用など、幹細胞に関するあらゆる疑問にお答えします。医療の未来を変える幹細胞の可能性を探ります。
幹細胞の基本的な定義
幹細胞とは、体のあらゆる組織や臓器の元となる特殊な細胞です。その最大の特徴は、自分と同じ細胞を作り出す「自己複製能」と、様々な種類の細胞に変化する「分化能」を持っていることです。つまり、幹細胞は私たちの体の「原材料」とも言える存在なんです。
なぜ幹細胞が注目されているのか
幹細胞が医学界で大きな注目を集めている理由は主に以下の3つです:
- 再生医療への応用: 損傷した組織や臓器を修復・再生する可能性を秘めています。例えば、脊髄損傷や心臓病、糖尿病などの治療に大きな期待が寄せられています。
- 疾患メカニズムの解明: 幹細胞を使って病気のモデルを作ることで、難病のメカニズム解明や新薬の開発に役立てられています。
- 個別化医療の実現: 患者さん自身の細胞から作られたiPS細胞を使うことで、その人に最適な治療法を見つけ出すことができるかもしれません。
これらの可能性により、幹細胞は「21世紀の医療を変える」と言われるほど、大きな期待が寄せられているんです。
幹細胞の種類
胚性幹細胞 (ES細胞)
ES細胞は、受精後3〜5日の初期胚(胚盤胞)の内部細胞塊から作られる幹細胞です。最大の特徴は、体のあらゆる細胞に分化できる「全能性」を持っていることです。
しかし、ヒトの胚を使用するため、倫理的な問題が議論となっています。
成体幹細胞
私たちの体の中にもともと存在している幹細胞です。主に組織や臓器の修復・維持に役立っています。例えば:
- 造血幹細胞(血液細胞を作る)
- 神経幹細胞(脳や神経系の細胞を作る)
- 間葉系幹細胞(骨、軟骨、脂肪などを作る)
成体幹細胞は、ES細胞ほどの多様性はありませんが、倫理的な問題が少ないのが特徴です。
人工多能性幹細胞 (iPS細胞)
2006年に京都大学の山中伸弥教授によって開発された、革新的な幹細胞です。成熟した体細胞(例えば皮膚の細胞)に特定の遺伝子を導入することで、ES細胞のような多能性を持つ細胞に戻すことができます。患者さん自身の細胞から作れるため、拒絶反応の心配が少なく、倫理的な問題も回避できるのが大きな利点です。
幹細胞の特徴
自己複製能
幹細胞の最も重要な特徴の一つが「自己複製能」です。これは、細胞分裂を繰り返しても、幹細胞としての性質を保ったまま増殖できる能力のことです。
例えば、1つの幹細胞が分裂すると、1つは幹細胞のままで、もう1つは分化していく細胞になります。この能力によって、幹細胞は体内で長期間にわたって維持され、必要に応じて新しい細胞を供給できるんです。
分化能
もう一つの重要な特徴が「分化能」です。これは、様々な種類の細胞に変化できる能力のことです。幹細胞の分化能には、いくつかのレベルがあります。
- 全能性: 胚のごく初期の細胞が持つ能力で、胎盤を含む全ての細胞に分化できます。
- 多能性: ES細胞やiPS細胞が持つ能力で、体を構成するほぼ全ての種類の細胞に分化できます。
- 多分化能: 成体幹細胞が持つ能力で、特定の組織や臓器の細胞に分化できます。
この分化能により、幹細胞は体の様々な部分の細胞を作り出し、組織や臓器の形成、修復、維持に貢献しているんです。
幹細胞の働き
体内での役割
幹細胞は、私たちの体の中で重要な役割を果たしています。
- 組織の形成: 発生過程で、幹細胞は分裂・分化を繰り返して体の各部分を形作ります。
- 組織の維持: 成体になっても、幹細胞は常に新しい細胞を供給し、組織や臓器の機能を維持します。
- 恒常性の維持: 幹細胞は体内環境の変化に応じて、必要な細胞を適切に供給し、体の恒常性を保ちます。
例えば、造血幹細胞は骨髄の中で日々約1000億個もの血液細胞を作り出し、私たちの体を支えているんです。
組織の修復と再生
幹細胞は、体の修復システムの要とも言える存在です。
- 傷の治癒: 皮膚に傷ができると、皮膚幹細胞が活性化して新しい皮膚細胞を作り出し、傷を修復します。
- 骨折の回復: 骨が折れると、骨幹細胞が活性化して新しい骨細胞を作り、骨を修復します。
- 筋肉の再生: 筋肉が損傷を受けると、筋衛星細胞(筋肉の幹細胞)が活性化して新しい筋細胞を作り出します。
この驚くべき修復能力は、幹細胞研究者たちが再生医療の実現に向けて研究を進める大きな動機となっているんです。
幹細胞のホーミング効果
幹細胞の組織修復・再生能力の中でも特に注目されているのが「ホーミング効果」です。これは、体内に投与された幹細胞が、損傷を受けた組織や炎症部位に自ら移動して集まる現象のことを指します。
ホーミング効果のメカニズムは以下のようなものです。
- 損傷部位からの信号: 組織が損傷を受けると、その部位から特定のケモカイン(化学物質)が放出されます。
- 幹細胞の反応: 幹細胞の表面には、これらのケモカインを認識する受容体が存在します。
- 幹細胞の移動: ケモカインを感知した幹細胞は、その濃度勾配に沿って損傷部位へと移動します。
- 組織への定着: 損傷部位に到達した幹細胞は、その場所に定着し、損傷部位の修復や再生を開始します。
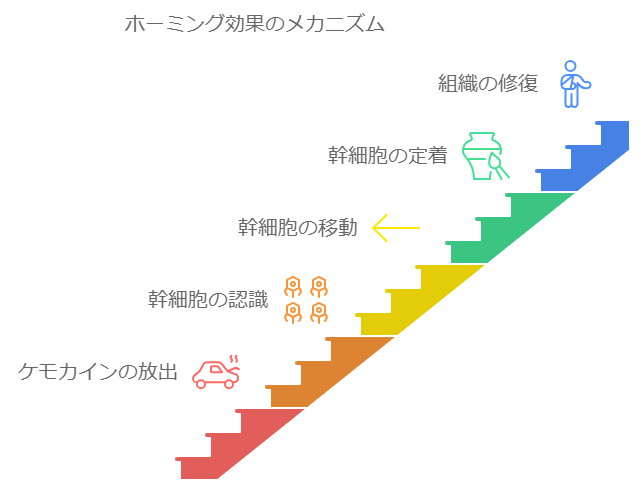
このホーミング効果は、再生医療において非常に重要です。
- 効率的な治療: 幹細胞が自ら損傷部位を見つけて移動するため、ピンポイントでの治療が可能になります。
- 副作用の軽減: 必要な場所にのみ幹細胞が集まるため、他の健康な組織への影響を最小限に抑えられます。
- 全身性疾患への応用: 複数の部位に問題がある場合でも、投与された幹細胞が各部位に適切に分布する可能性があります。
現在、このホーミング効果を利用した治療法の研究が進められています。例えば、心臓病や脳梗塞、糖尿病などの治療に応用されることが期待されているんです。
ただし、ホーミング効果をより効果的に引き出す方法や、目的の組織へのホーミングを確実にする技術など、まだ解決すべき課題も多く残されています。
幹細胞研究の歴史
主要な発見と進歩
幹細胞研究の歴史は、医学の進歩と密接に関わっています。
- 1960年代: カナダのジェームズ・ティルとアーネスト・マッカロックが、マウスの骨髄細胞の中に血液細胞を作り出す能力を持つ細胞(造血幹細胞)が存在することを発見。
- 1981年: マーチン・エバンスとマシュー・カウフマンが、マウスのES細胞の分離に成功。
- 1998年: ジェームズ・トムソンらのチームが、ヒトのES細胞の生成に成功。
- 2006年: 山中伸弥らのチームが、マウスの皮膚細胞からiPS細胞の作製に成功。
- 2007年: 山中らのチームと、ジェームズ・トムソンらのチームが、それぞれ独立してヒトのiPS細胞の作製に成功。
これらの発見により、幹細胞研究は飛躍的に進歩し、再生医療の実現に向けて大きく前進しました。
ノーベル賞受賞研究
幹細胞研究の重要性は、複数のノーベル賞受賞によっても認められています。
- 2007年ノーベル生理学・医学賞: マーチン・エバンス、マリオ・カペッキ、オリバー・スミシーズが、ES細胞を使ったマウスの遺伝子改変技術の開発により受賞。
- 2012年ノーベル生理学・医学賞: 山中伸弥とジョン・ガードンが、成熟細胞の初期化に関する発見により受賞。山中のiPS細胞の発見が高く評価されました。
これらの受賞から、幹細胞研究が現代医学において非常に重要な研究であると認められていることが分かります。
幹細胞の医療応用
再生医療での利用
幹細胞を用いた再生医療は、従来の治療法では難しかった疾患や障害に対する新たな希望となっています。
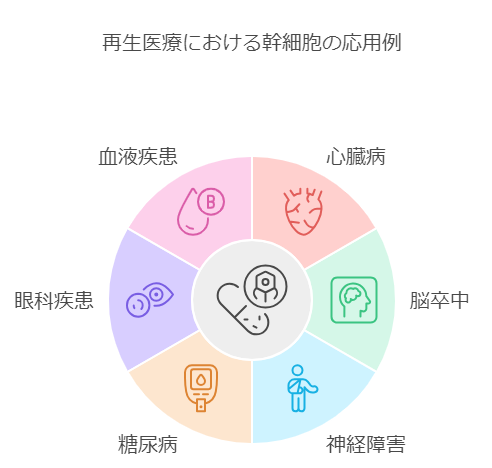
- 心臓病: 心筋梗塞後の心臓組織の再生に、骨髄由来の間葉系幹細胞やiPS細胞由来の心筋細胞が使用されています。
- 神経疾患: パーキンソン病やアルツハイマー病、脊髄損傷などの治療に、神経細胞への分化能が高い骨髄由来幹細胞による治療が行われています。
- 脳梗塞: 脳梗塞後の神経機能回復を目指し、骨髄由来の間葉系幹細胞や神経幹細胞を用いた治療が行われています。
- 糖尿病: 1型糖尿病の治療として、脂肪由来幹細胞を用いた幹細胞点滴治療が行われています。
- 眼科疾患: 加齢黄斑変性や網膜色素変性症などの治療に、iPS細胞由来の網膜色素上皮細胞の移植が臨床試験段階に入っています。
- 血液疾患: 白血病などの治療に、造血幹細胞移植が既に広く行われています。
これらの治療法は、まだ多くが研究段階や臨床試験の段階にありますが、一部はすでに実用化されており、今後の発展が大いに期待されています。
疾患モデルとしての活用
幹細胞、特にiPS細胞は、病気のメカニズムを解明するための強力なツールとなっています。
- 難病の病態解明: 患者さんのiPS細胞から病気の細胞を作り出し、その挙動を観察することで、難病のメカニズムを解明できます。
- 個別化医療への応用: 患者さん個人のiPS細胞を用いることで、その人特有の病態や薬の効果を予測することができます。
- 発生・分化の研究: ES細胞やiPS細胞を用いて、人間の発生や細胞分化のプロセスを詳細に研究することができます。
例えば、ALS(筋萎縮性側索硬化症)やアルツハイマー病など、これまで研究が困難だった神経疾患の病態解明に、iPS細胞由来の神経細胞が大きく貢献しています。
創薬研究での応用
幹細胞技術は、新薬開発のプロセスを大きく変えつつあります。
- 薬効評価: ヒトのiPS細胞由来の細胞を使用することで、動物実験よりも精度の高い薬効評価が可能になります。
- 毒性試験: 肝臓や心臓など、薬物代謝に関わる重要な臓器の細胞を幹細胞から作り出し、新薬の安全性を効率的に評価できます。
- 個別化医療のための薬剤スクリーニング: 患者さん個人のiPS細胞を用いて、その人に最も効果的な薬剤を選別することができます。
これらの応用により、新薬開発のコストと時間を大幅に削減できる可能性があります。また、より安全で効果的な薬の開発が期待されています。
幹細胞と美容・アンチエイジング
幹細胞技術は医療分野だけでなく、美容やアンチエイジングの世界でも大きな注目を集めています。若々しさや美しさの維持に幹細胞を活用しようという試みが、様々な形で展開されているんです。
幹細胞コスメ
近年、「幹細胞コスメ」という言葉をよく耳にするようになりました。これらの製品は大きく二つに分類されます。
- 植物由来の幹細胞エキスを含む製品:
- リンゴやブドウなどの植物の幹細胞から抽出したエキスを含んでいます。
- 抗酸化作用や細胞の活性化効果が謳われていますが、科学的な裏付けは限定的です。
- ヒト幹細胞培養液を含む製品:
- ヒトの幹細胞(多くは脂肪由来幹細胞)を培養した際の培養液(上澄液)を含んでいます。
- 成長因子やサイトカインなどの有効成分が含まれていると言われています。
これらの製品の効果については、まだ科学的な検証が十分ではありません。過度な期待は禁物ですが、一部の製品では肌の状態改善に効果があるという報告もあります。
幹細胞を活用した美容医療
美容医療の分野では、幹細胞を直接利用した治療法が研究・実施されています。
- 脂肪幹細胞を用いた治療:
- 患者さん自身の脂肪組織から取り出した幹細胞を利用します。
- 顔のしわやたるみの改善、傷跡の修復などに使用されています。
- 自己由来の細胞を使用するため、副作用などのリスクが相対的に低いと考えられます。
- 毛髪再生治療:
- 頭皮の幹細胞を活性化させることで、毛髪の成長を促進する治療法が研究されています。
- 一部の医療機関では、すでに治療が始まっています。
幹細胞とアンチエイジング研究
幹細胞は、アンチエイジング研究の最前線でも重要な役割を果たしています。
- 老化メカニズムの解明:
- 加齢に伴う幹細胞の機能低下のメカニズムを研究することで、老化現象そのものについての研究が促進されています。
- 若返りの可能性:
- 若い個体の血液や幹細胞を老いた個体に投与することで、一部の組織で若返りの効果が見られるという研究結果があります。
- 組織再生:
- 加齢とともに機能が低下した組織や臓器を、幹細胞を用いて再生させる研究が進められています。
ただし、これらの研究はまだ初期段階にあり、人間での効果や安全性については、さらなる検証が必要です。また、「若返り」や「不老」を目指す研究には、倫理的な議論も伴います。
幹細胞研究の課題と倫理的問題
技術的な課題
幹細胞研究には、まだ多くの技術的な課題が残されています。
- 分化制御: 幹細胞を目的の細胞に効率よく・純度を高く分化させる技術の向上が必要です。
- 腫瘍化リスク: 特にES細胞やiPS細胞を用いた治療では、移植後の腫瘍形成リスクを無くす必要があります。
- 免疫拒絶反応: 他人の細胞由来の幹細胞を使用する場合、免疫拒絶反応を抑制する技術が必要となります。
- 大量培養と品質管理: 臨床応用に必要な大量の細胞を、安定した品質で培養する技術の確立が求められています。
これらの課題に対して、世界中の研究者が日々新しい解決策を模索しています。
倫理的な議論
幹細胞研究、特にヒトES細胞研究には、様々な倫理的な問題が議論されています。
- 胚の扱い: ES細胞の作製には胚の破壊が伴うため、生命の始まりをどう定義するかという根本的な問題があります。
- 卵子提供の問題: 研究用のES細胞作製には女性からの卵子提供が必要で、その過程での倫理的な配慮が必要となります。
- 遺伝子改変: 幹細胞の遺伝子を改変することで、「デザイナーベビー」につながる可能性への懸念があります。
- 経済的格差: 高額な幹細胞治療が、経済的に余裕のある人にしか受けられないという問題があります。
これらの倫理的問題に対しては、各国で法律や指針が設けられていますが、科学の進歩とともに常に新たな議論が生まれています。
宗教的な問題も絡むため、今後も様々な議論が行われるでしょう。
幹細胞と他の先端医療技術との関連
幹細胞研究は単独で進んでいるわけではありません。他の先端医療技術と融合することで、さらに大きな可能性を開いています。
ここでは、幹細胞研究と密接に関連する他の先端医療技術について見ていきましょう。
遺伝子治療との連携
幹細胞と遺伝子治療の組み合わせは、多くの遺伝性疾患の治療に新たな可能性を開いています。
- 遺伝子治療:
- 患者から採取した幹細胞に治療用遺伝子を導入し、体外で増やした後に体内に戻す方法。
- 例:重症複合免疫不全症(SCID)の治療で実用化されています。
- ゲノム編集技術との組み合わせ:
- CRISPR-Cas9(クリスパー・キャスナイン)などの技術を用いて、より精緻な遺伝子修復が期待できます。
- 例:鎌状赤血球症などの血液疾患の治療研究が進んでいます。
免疫療法との連携
幹細胞技術は、がん免疫療法の分野でも重要な役割を果たしています。
- CAR-T細胞療法:
- T細胞(免疫細胞の一種)に、がん細胞を特異的に認識する受容体(CAR)を導入する治療法。
- iPS細胞由来のT細胞を使用することで、より効率的で安全なCAR-T細胞の作製が可能になると期待されています。
- がんワクチン:
- 樹状細胞(免疫細胞の一種)を用いたがんワクチンの研究が進んでいます。
- iPS細胞から作製した樹状細胞を使うことで、より効果的なワクチンの開発が期待されています。
再生医療とAI技術
人工知能(AI)技術は、幹細胞研究と再生医療の様々な場面で活用されています。
- 細胞の品質評価:
- 機械学習を用いて、iPS細胞の品質を高速かつ正確に評価する技術が開発されています。
- 分化プロトコルの最適化:
- AIを使って、幹細胞から目的の細胞への分化を最適化する研究が進んでいます。
ナノテクノロジーとの融合
ナノテクノロジーは、幹細胞の培養や移植、薬剤デリバリーなどの分野で重要な役割を果たしています。
- ナノ材料を用いた足場:
- ナノファイバーなどを用いて、より生体に近い環境で幹細胞を培養する技術が開発されています。
- ナノパーティクルを用いた薬剤・遺伝子デリバリー:
- 幹細胞に特異的に薬剤や遺伝子を導入する技術の開発が進んでいます。
- ナノセンサー:
- 幹細胞の状態をリアルタイムでモニタリングするナノスケールのセンサーの開発が進められています。
これらの先端技術と幹細胞研究の融合により、医療の未来は大きく変わろうとしています。一つ一つの技術が進歩するだけでなく、それらが組み合わさることで、想像以上の相乗効果が生まれる可能性があるんです。
ただし、これらの技術の多くはまだ研究段階にあり、実用化までには更なる研究と時間が必要です。また、新しい技術の登場に伴い、倫理的・社会的な課題にも目を向ける必要があるでしょう。
まとめ
幹細胞研究は、現代医学の最前線に立つ革新的な分野です。この記事を通じて、幹細胞の基本的な概念から最新の研究動向まで、幅広く探ってきました。ここで、主要なポイントを振り返ってみましょう。
幹細胞研究の現状
- 幹細胞には、ES細胞、成体幹細胞、iPS細胞など、様々な種類があり、それぞれにメリット・デメリットがあります。
- 幹細胞の持つ自己複製能と分化能は、再生医療の基盤となる重要な特性です。
- 幹細胞研究は、再生医療だけでなく、疾患モデルの作製や創薬研究にも広く応用されています。
幹細胞研究の可能性
- 難治性疾患や遺伝性疾患に対する新たな治療法の開発が期待されています。
- 個別化医療の実現に向けて、幹細胞技術は重要な役割を果たすでしょう。
- 臓器移植の代替手段として、幹細胞から作製した組織や臓器の利用が期待されています。
- 美容・アンチエイジング分野でも、幹細胞技術の応用が進んでいます。
直面する課題
- 安全性の確保、特にiPS細胞を用いた治療における腫瘍化リスクの排除が重要課題です。
- 治療コストの削減や、大量培養技術の確立など、実用化に向けた技術的課題が残されています。
- ES細胞研究やゲノム編集技術の利用に関しては、倫理的な議論が続いています。
社会への影響
幹細胞研究の進展は、医療の枠を超えて社会全体に大きな影響を与える可能性があります。医療費の削減、健康寿命の延伸、新産業の創出など、その影響は多岐にわたるでしょう。同時に、生命の定義や人間の本質に関する深い哲学的、倫理的な問いも投げかけています。
最後に
幹細胞研究は、人類の健康と福祉に大きな貢献をする可能性を秘めた、希望に満ちた分野です。しかし、その実現には科学的な画期的な成果だけでなく、社会全体での対話と合意形成が不可欠です。
私たち一人一人が幹細胞研究について理解を深め、その可能性と課題について考えることが重要です。科学の進歩と倫理的配慮のバランスを取りながら、この革新的な技術を人類の幸福のために最大限に活用していく。そんな未来を築いていくために、幹細胞研究は今日も進化を続けているのです。
私たちは今、医学の歴史に残る大きな変革の瞬間に立ち会っているのかもしれません。
#幹細胞 #再生医療 #幹細胞治療
よくある質問 (FAQ)
- Q: 幹細胞治療は安全ですか?
A: 幹細胞治療の安全性は、使用する幹細胞の種類や治療法によって異なります。現在、多くの臨床試験が行われており、安全性の確保に向けた研究が進められています。ただし、特にiPS細胞を用いた治療では、腫瘍化のリスクなど、まだ克服すべき課題があります。 - Q: 幹細胞治療はどんな病気に効果がありますか?
A: 現在、血液疾患、一部の眼疾患、一部の皮膚疾患などで幹細胞治療が実用化されています。また、心臓病、神経変性疾患、糖尿病など、様々な疾患に対する治療法の研究が進んでいます。 - Q: iPS細胞とES細胞の違いは何ですか?
A: iPS細胞は成熟した体細胞から作られるのに対し、ES細胞は受精卵から作られます。iPS細胞は倫理的な問題が少なく、患者自身の細胞から作れるという利点がありますが、ES細胞の方が研究の歴史が長く、性質がよく分かっているという面があります。 - Q: 幹細胞研究にはどんな倫理的問題がありますか?
A: 主な倫理的問題として、ES細胞研究における胚の使用、ゲノム編集技術との組み合わせによる遺伝子改変の是非、幹細胞治療の公平な利用機会の確保などがあります。 - Q: 幹細胞研究は今後どのように発展していくと予想されますか?
A: 今後は、オルガノイド研究の発展による複雑な組織・臓器の作製、AIとの融合による効率的な創薬、ゲノム編集技術との組み合わせによる遺伝子疾患の治療など、様々な分野での 技術革新が期待されています。同時に、倫理的・社会的な議論も深まっていくでしょう。
